微流控制備仿佛珠微載體用于細胞培養研究
瀏覽次數: 342 發布時間:2017-09-18 09:26:29 發布人:editor
近年來,三維細胞培養在模擬體內細胞與細胞、細胞與微環境之間的相互作用方面取得了不錯的技術進步,進一步鞏固了其在組織工程領域的重要地位。而細胞微載體,作為一種新型的適用于細胞三維培養的仿生平臺,它為細胞的包裹以及細胞球聚體的形成提供了三維的生物材料支架。光刻、微模板、電噴、微流控等方法都可用于細胞微載體的制備。其中,微流控方法制備細胞微載體具有單分散性高、尺寸控制精準、高通量、細胞微環境可控等優點,是一種相當具有前景的三維細胞包裹技術。
然而,由于缺少有效的營養交換途徑,絕大多數的細胞微載體尺寸都限制在一定范圍內,以避免載體內部細胞的壞死。此外,傳統的細胞微載體只能夠為細胞提供均一的微環境,而體內的細胞分布是十分復雜的。空間各向異性或異質的組織在生物體內普遍存在,其對保持生物體的生理功能具有重要意義。因此,賦予微載體更多復雜的結構和功能,并且實現氧氣營養物質充分交換值得期待。
【成果簡介】
近日,東南大學趙遠錦教授課題組在Science China Materials上發表了一篇題為Microfluidic generation of Buddha beads-like microcarriers for cell culture的封面文章。文中報道了一種受佛珠手串中佛珠可以在繩子上自由滑動這一特殊結構的啟發,利用毛細管陣列微流控技術制備的具有可控大孔微結構的新型異質細胞微載體,用于細胞三維培養研究。仿佛珠微載體的構建首先需要通過海藻酸鈉與鈣離子的快速凝膠化形成海藻酸鈣纖維,隨即在纖維上包覆可聚合的細胞預聚溶液,通過流體的剪切實現溶液乳化并將其固化聚合,從而獲得串有可以自由滑動的微載體的纖維串。纖維上釋放的微載體中間的大孔結構的尺寸高度可控,這一特點在微載體用于細胞三維培養中具有重要意義,因為微載體中間的大孔結構能夠有效保證載體內部細胞氧氣、營養物質的充分交換,減少細胞壞死。此外,通過將多種細胞預聚溶液引入微流控通道中,還可以獲得具有多組分異質結構的細胞微載體,從而有望實現體內復雜的組織器官結構與功能的模擬。
【圖文導讀】
圖一:受佛珠啟發的大孔微載體微流控制備示意圖
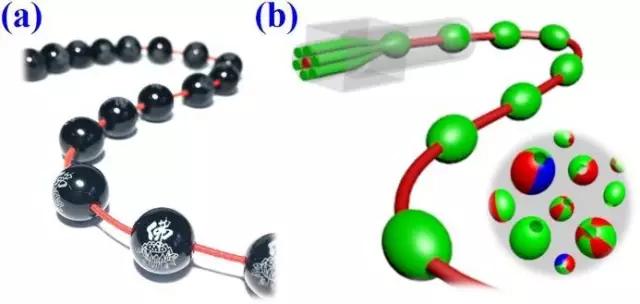
圖1.(a)佛珠手串;
(b)毛細管陣列微流控技術制備大孔微載體。
圖二:大孔微載體的可控制備
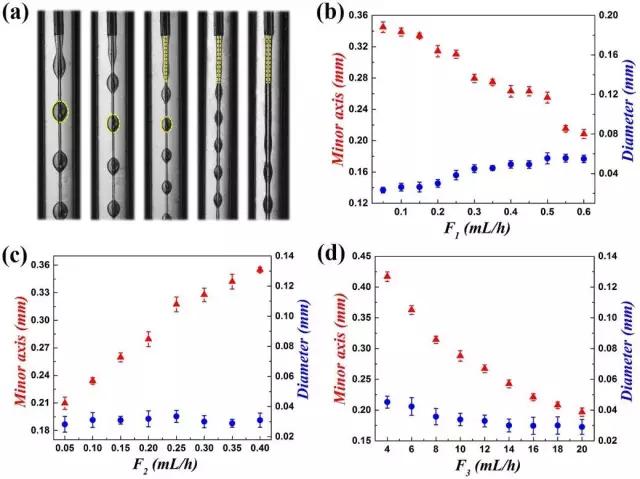
圖2.(a)尺寸可控的包覆有液滴的微纖維實時微流控生成圖;
(b-d)液滴短軸長(紅點)和纖維直徑(藍點)與內相(F1)、中間相(F2)和外相(F3)流速的關系。
圖三:微纖維表征

圖3. 微纖維的(a-c)共聚焦圖片和(d)電鏡圖表征;
(e-f)利用微載體在纖維上可滑動的特性所展示的同一組微纖維上的載體分散、堆疊狀態下的光鏡圖。
圖四:微載體表征
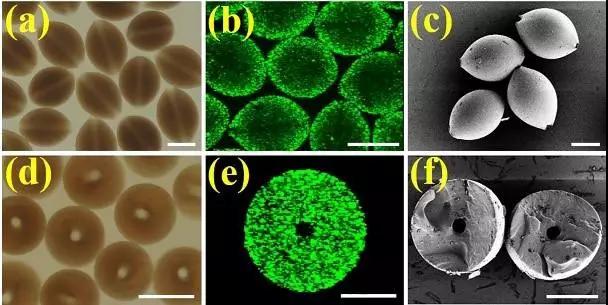
圖4.(a-c)大孔微載體的光鏡、共聚焦以及電鏡圖表征;
(d-f)大孔微載體橫截面的光鏡、共聚焦以及電鏡圖表征。
圖五:多組分微載體的微流控制備示意圖和共聚焦表征

圖5.(a)兩組分,(b)三組分和(c)六組分的微載體的微流控制備示意圖和共聚焦表征。
圖六:大孔微載體與實心微載體對包裹的細胞活性的比較
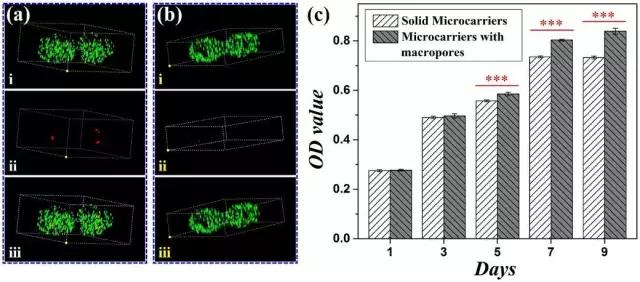
圖6.(a)實心微載體以及(b)大孔微載體培養七天的細胞活死染;
(c)實心微載體以及大孔微載體MTT表征。
圖七:兩組分微載體在細胞共培養方面的研究
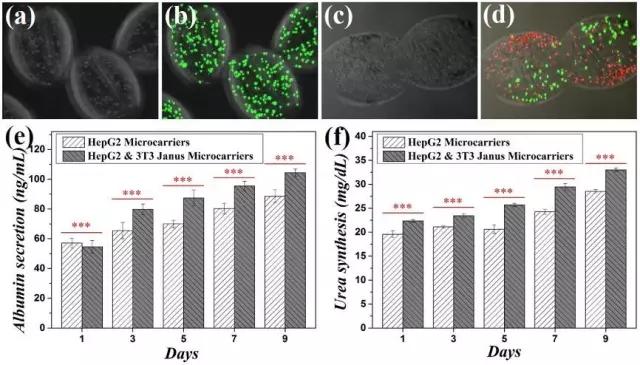
圖7.(a-d)一組分和兩組分的大孔微載體的光鏡和共聚焦表征;
(e)微載體的白蛋白分泌;
(f)微載體的尿素合成。
【小結】
本研究提出了一種利用毛細管陣列微流控技術連續制備串有可移動大孔微載體的微纖維的途徑。與佛珠可從手串繩子上滑動、脫落這一特點類似,微載體可以從微纖維上剝離且不破壞載體結構,這得益于微載體在纖維上的可移動性。通過調節微流控流體的各相流速,微載體及其內部的大孔尺寸高度可控;這保證了細胞包裹和培養過程中的氧氣營養物質的充分交換。此外,通過將多種細胞預聚溶液引入微流控通道中,還可以獲得具有多組分異質結構的細胞微載體;在微載體中將肝實質細胞與成纖維細胞共培養,可以觀察到肝臟特異性功能的高水平表達,進一步論證了微載體的優越性。因此,研究人員認為,這些載有細胞的微載體可以用作生物體中的生物模型甚至是更為復雜的多組織研究,有望實現人體較大器官網絡行為的模擬研究。
